製薬 vs バイオテクノロジー (化学 vs 生物学)
バイオテクノロジーと医薬品はしばしば混同されます。 どちらも薬を生産していますが、その方法と根拠は異なります。 医薬品を製造するために、バイオテクノロジー企業は細菌などの生きた生物を使用しますが、製薬業界は通常、人工材料を使用して医薬品を製造します。
バイオテクノロジー企業は他の業界とどう違うのですか?
バイオテクノロジーは、医薬品やその他の薬物に加えて、農薬の量を減らしたり、栄養価を高めたりするなど、作物を開発するために農薬産業でも使用されているため、より広い用途を持っています。
さらに、バイオテクノロジーは研究開発により重点を置く傾向がありますが、製薬会社は通常、医薬品をより大きな商業規模で製造することに重点を置いています。
バイオテクノロジー企業は、収益の 40 ~ 50% を研究に投資しています。
研究の量が多いため、バイオテクノロジー業界では開発プロセスが長くなり、その結果、より高いコストが発生します。 WIPO によると、バイオテクノロジー企業は収益の 40 ~ 50% を研究に投資しているため、結果の保護が大きな問題になっています。
バイオテクノロジー企業は、市場の可能性を秘めた画期的なイノベーションを目指しており、それを製薬会社にライセンス供与できます。 したがって、その結果を保護し、競合他社にコピーされる前に特許で活用することが重要です。
特許性に関する法律
バイオテクノロジーの性質を考えると、自然に発生する生物の使用は、開発の特許性を取り巻く多くの法律を生み出しました. この問題は通常、診断テストで発生します。
Ariosa Diagnostics v Sequenom (2015) では、主題は 101 年特許法第 1952 条に基づいて特許可能ではないと判断されました。 これは自然に発生する現象であり、進歩性を伴わないため、特許を受けることはできませんでした。
この判決は、以前の事件、Mayo v Prometheus Labs (2012) によって支持されました。 この場合、Prometheus Labs は、胃腸疾患を治療するための薬物治療の適切な投与量をテストするための手順の特許を取得し、独自の同様のテストを使用しようとしたときに Mayo を訴えました。
米国の連邦判事は、特許を無効にし、特許は薬物に対する体の反応をカバーすることはできないと述べた.
特許は、薬物に対する身体の反応をカバー[できない].
米国最高裁判所は、下級裁判所の判決を覆し、テストに含まれるプロセスは特許の対象とならない自然法則であると判断しました。 プロメテウスがアプリケーションに追加したステップは、自然の法則を適用するための単なる指示でした. 裁判所は、自然法則に関する特許を許可すると、さらなる発見が妨げられるとの判決を下しました。 裁判所は次のように述べています。
「そのような決定を行う方法は当技術分野でよく知られているため、このステップは、以前はこの分野の科学者が行っていた、よく理解された日常的な従来の活動に従事するように医師に指示するだけです. そのような活動は、通常、特許を取得できない自然法則をそのような法律の特許適格な適用に変換するには十分ではありません。」
したがって、次のように結論付けられました。
- 新たに発見された自然法則は特許を受けることができない
- 新たに発見された法律の適用は、その適用がその分野ですでに知られている要素に依存している場合、通常は特許を受けることができません。
これらの問題は、多くのバイオテクノロジー企業がその結果が特許可能であることを保証するために考慮する必要があります。
製薬業界が直面する特許問題
リチャード・レビンらとウェス・コーエンらによる研究では、イノベーションから利益を得る上でどの要因が最も重要であるかを特定するために、業界の大部分で米国の研究開発専門家を対象に調査を実施しました。
調査によると、次の要因が含まれていることがわかりました。
- 競争力
- 最初に市場に投入
- 優れた販売
- 特許
どちらの研究も、製薬業界が他のどの業界よりも特許を重視していることを示しています。
製薬業界は他のどの業界よりも特許を重視しています
製薬会社が薬の特許を申請して市場に出すと、その薬を独占的に販売する権利が与えられ、事実上の独占が得られます。 製薬会社もまた、研究開発プロセスが長く、FDA の承認や臨床試験を経なければならないため、多くの費用がかかります。
Tufts Center for the Study of Drug Development の調査によると、新薬の開発にかかる平均コストは 800 億ドル (648 億 XNUMX 万ポンド) を超えています。 これらのコストを回収する企業の能力は、開発と販売の供給を制御する能力に大きく依存しています。
ジェネリック医薬品会社
医薬品の特許が失効すると、特許権者は独占権を保持できなくなり、ジェネリック医薬品会社がその医薬品の製造と販売を開始できるようになります。
この時点で、ジェネリック医薬品会社は、医薬品を低コストで迅速に活用および再生産し、はるかに競争力のある価格で販売できるため、市場で優位に立つことができます。
アメリカの製薬大手ファイザーは、バイアグラとして知られているシルデナフィルの特許を米国でまだ保持していますが、EU の特許は 2013 年に失効しました。 一方、韓国では、Hanmi Pharmaceutical がこの地域で有効期限が切れた後、ファイザーの価格の 28 分の 1.98 である 4.25 ドル (3.50 ポンド) で薬を販売し始めました。
IP が重要になるのはいつですか?
製薬会社とバイオテクノロジー会社の両方が、研究開発中に特許調査を実施する必要があります。 ただし、このプロセスのどの時点で行うかは、業界によって異なります。 バイオテクノロジー企業は、生物の研究に多くの時間を費やして特許性のある結果を見つけているため、特許検索は通常、製薬会社よりもはるかに遅い段階にあります。
さらに、バイオテクノロジー企業と製薬企業が特許を取得した医薬品の製造と流通に与えられる期間には大きな違いがあります。 米国では、バイオテクノロジー企業の特許保護期間は 12 年と長く、製薬会社は毎年の強制更新に直面するまでにわずか XNUMX 年しかありません。
この不一致は、長い FDA 承認プロセスのために生物学的医薬品を市場に出すというかなりの困難によるものです。 当初、特許の延長は、米国のハッチ ワックスマン法を通じてバイオテクノロジー企業に付与されていました。 これにより、失われた特許存続期間を補うための延長が提供されました。 その後、米国議会は、バイオテクノロジー企業が生物学的製品の規制データを 12 年間保護できるシステムを採用しました。 製薬会社には生物学的根拠がないため、これは当てはまりません。
業界にまたがる
特許は、業界を超えたアプリケーションにも非常に重要です。 過去数年間のエネルギー生産へのバイオテクノロジーの貢献は、十分に文書化されています。 国際エネルギー機関によると、世界のバイオ燃料生産は 2000 年から 2007 年の間に 2015 倍になりました。40.9 年には、バイオテクノロジー産業によるエネルギー生産への最大の貢献はエタノール生産であり、33.1 年に生み出された 2014 億ドル (XNUMX 億ポンド) の収益をさらに上回りました。
上記のように、バイオテクノロジーは農業産業でも頻繁に使用され、農薬耐性があり、栄養価や収量が増加した新しい植物や動物を生産または商品化しています。 IP 保護がなければ、製品の商品化は冗長になる可能性があります。
製薬会社にとって、バイオテクノロジー企業、研究機関、または大学からの既存の特許技術および製品を調査することは、どの開発を商業化するかを特定する能力を提供します。 あるいは、製薬会社が独自の合成薬を開発している場合、特定のポリマーや化合物がすでに存在するかどうかを識別する能力は非常に重要です。
製薬企業やバイオテクノロジー企業の戦略的目標を、特許検索でどのようにサポートできるでしょうか?
特許保護はイノベーションを保護し、競合他社が市場で模倣するのを防ぐために重要ですが、市場でのアイデアの可能性を正確に理解することで、何億もの研究費を節約できます。
第二に、医薬品や製品が FDA によって承認されると、その潜在的なアプリケーションを調べることができるため、R&D の目的に優先順位を付ける上で大きな価値があります。 バイオテクノロジーの最終的な目標は、製品を他の企業に商品化することです。 最も収益性の高い機会を見つけるために、特許検索により、同様の分野で活動している主要な組織を特定できます。これにより、市場のギャップが明らかになる可能性があります。
最後に、バイオテクノロジー企業は通常、製薬企業よりも規模が小さいため、多数のバイオテクノロジー企業の本拠地である研究拠点が集中しています。 製品が同時に生産された後に訴訟を起こす危険を冒すよりも、同僚が何を研究しているかを知ることで、衝突を回避し、コラボレーションの機会を提供できます。
まとめ
- バイオテクノロジーと製薬の主な違いは、有機と化学です
- 特許性はバイオテクノロジーの重要な問題です
- 新薬の開発にかかる平均コストは 800 億ドル (648 億 XNUMX 万ポンド) を超えています
- バイオテクノロジーの特許は 12 年間保護します。 製薬ジャストファイブ
- ジェネリック医薬品は特許切れ後、製薬会社にとって脅威となる
- 特許データは、費用のかかる訴訟リスクを軽減する上で重要です
ウェビナーを見る: 診断および治療に関する特許およびライセンス戦略.
脚注
- Henry Grabowski、デューク大学、「製薬およびバイオテクノロジー産業における特許と新製品開発」2002 年、p3 パラ 1。
- https://www.viamedic.com/blg/male-impotence/viagra/viagras-price-coming-down-sales-going-up
- カーリー・ヘルファンド「ファイザーのバイアグラ ブランドに対する今後のジェネリック医薬品の脅威はさらに恐ろしいものになりました」、Fierce Pharma、2015
あなたのおすすめコンテンツ
-
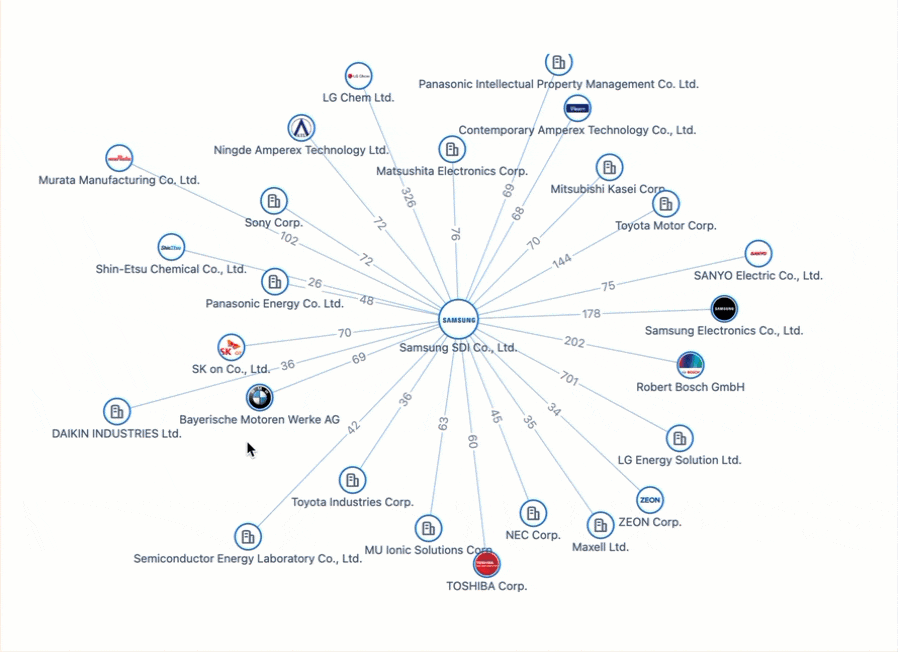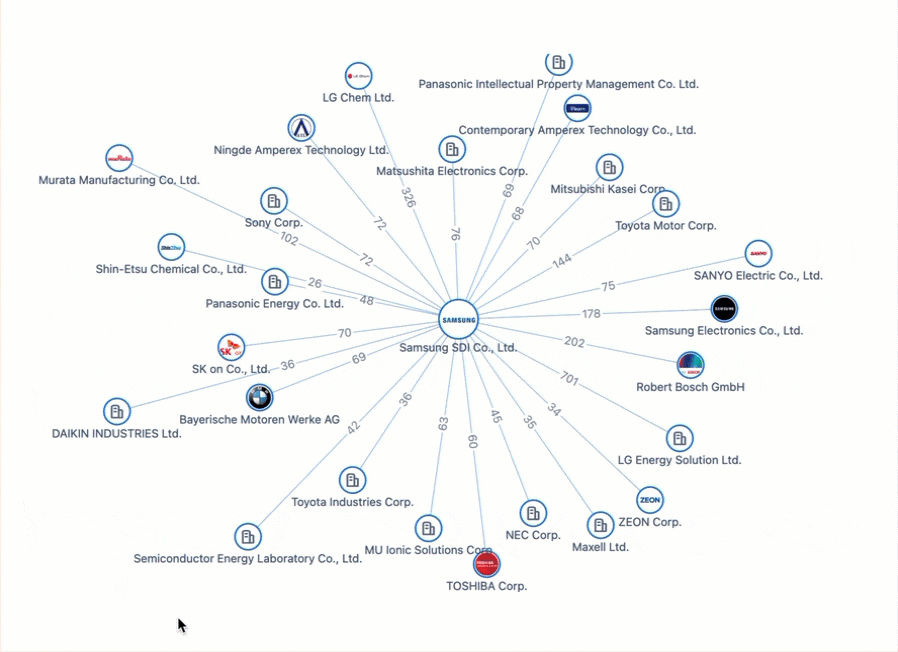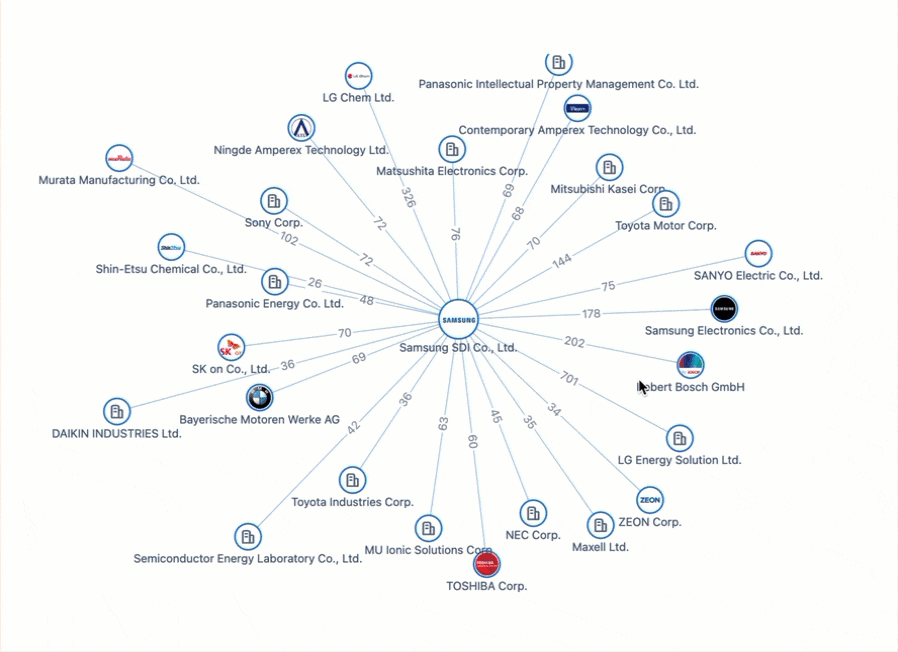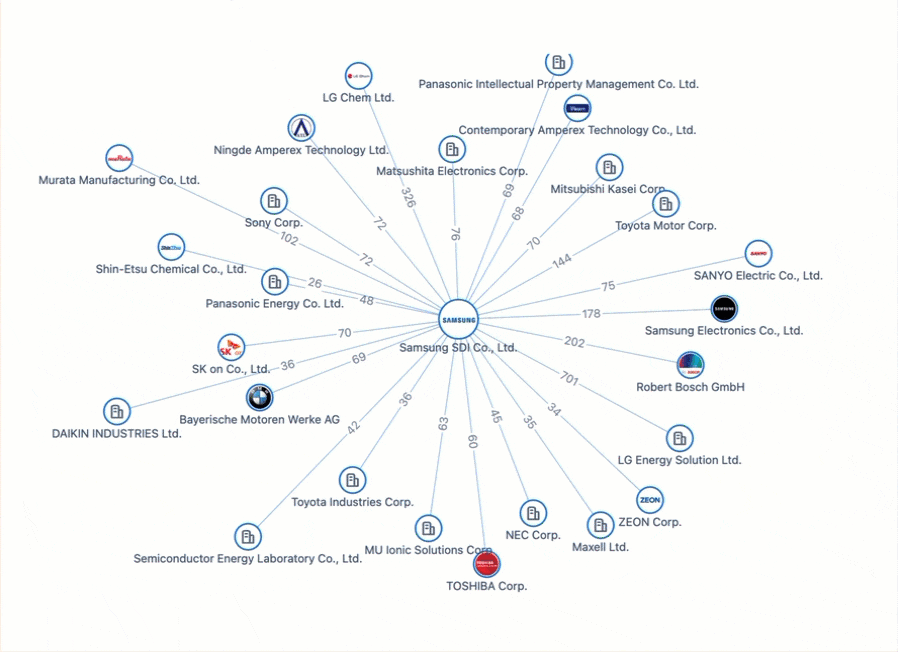
電気自動車の未来に電力を供給: バッテリーのイノベーションと特許をめぐる戦い
カテゴリー: 記事 | カテゴリー: バッテリー技術 | カテゴリー: 電気自動車 | カテゴリー: EV | カテゴリー: リチウムイオン | カテゴリー: リチウムイオン電池 | カテゴリー: ねえ | カテゴリー: 新エネルギー車
4月月曜日、22、2024
進化を続けるイノベーションの中で、電気自動車 (EV) 業界は技術変革の先駆けとなっています。 EV 革命を推進する特許を調査すると、Apple のベンチャー企業は、業界の巨人ですらこの競争分野で直面する課題の痛切な例として役立ちます。優れた電源ソリューションの探求が展開され、EV 革命の真の先駆者たちが名を残している世界的な特許情勢を巡る旅にご参加ください。
-

人間 vs. AI: 生成型人工知能の時代にアイデアを所有するのは誰ですか?
カテゴリー: AI時代 | カテゴリー: AI を活用した創造性 | カテゴリー: AIが生成した作品 | カテゴリー: 記事 | カテゴリー: 著作権と特許権 | カテゴリー: デジタルイノベーション | カテゴリー: 革新 | カテゴリー: 知的財産法 | カテゴリー: 法的な意味 | カテゴリー: OpenAI ソラ | カテゴリー: 特許法 | カテゴリー: 研究タグ | カテゴリー: ソーラ | カテゴリー: テキストからビデオへの生成 AI | カテゴリー: AIの所有者は誰か
4月月曜日、22、2024
テキストからビデオへの生成 AI モデルである OpenAI の Sora ソフトウェアは、最近、一連の 1 段落のプロンプトと、それらのプロンプトに基づいて生成された高品質の映像を示して見出しを飾りました。これは当然のことながら印象深いものですが、知的財産法が生成 AI によってどのように破壊されるかを特定するにはまだ時期尚早です。この社説は、Sora の影響の多面的な状況を掘り下げ、AI 時代のイノベーションとオーナーシップの将来についての洞察を提供します。
-

Patsnap が 2023 年のグローバル イノベーション レポートを発表: イノベーションのダイナミックな状況に輝かしい名前を付けたもの
カテゴリー: 記事 | カテゴリー: 電子ブック | カテゴリー: 研究タグ | カテゴリー: ホワイトペーパー
11月水曜日、15、2023
Global Innovation 100 と Global Disruption 50 は個々の組織を超えており、それぞれが多数の子会社を持つ小規模なイノベーション エコシステムを表しています。 これらの企業のイノベーション データを通じて、世界的なイノベーションの特徴、構造、傾向についての洞察が得られます。