FDA stellt neue Vorschriften für Tierversuche vor: Ein Schritt vorwärts in der Modernisierung der Wissenschaft
Sind Sie bereit für eine Revolution in der Arzneimittelprüfung? Seit Jahrzehnten verlangt die US-amerikanische Arzneimittelbehörde FDA (Food and Drug Administration) Tierversuche vor klinischen Studien am Menschen als Voraussetzung für die Zulassung neuer Medikamente auf dem Markt. Im Dezember 2022 kam es jedoch zu einer bahnbrechenden Veränderung. Präsident Joe Biden unterzeichnete ein neues Gesetz, das der FDA die Befugnis erteilt, Medikamente oder Biologika für Studien am Menschen auf der Grundlage von nicht-tierischen Testmethoden zuzulassen.
Dies ist ein bedeutender Schritt in Richtung Modernisierung der Wissenschaft und könnte den Beginn einer neuen Ära der Arzneimittelprüfung einläuten. Ist dies also der Beginn einer Transformation der pharmazeutischen Prüfung? Nur die Zeit wird es zeigen.
In diesem Artikel befassen wir uns mit der Geschichte der Tierversuche und alternativen Möglichkeiten.
Der Anfang und das Ende der Tierversuche der FDA
Die Debatte um Tierversuche in der Arzneimittelforschung dauert schon seit Jahrhunderten an. Zwar zielen die jüngsten Gesetze darauf ab, Tierversuche humaner zu gestalten, doch bleibt die Frage, ob Tiere die Reaktionen des Menschen auf Medikamente wirklich nachbilden können, weiterhin umstritten.
Erst als es 1937 zu einer tragischen Massenvergiftung durch ein neues Produkt kam, das ohne ordnungsgemäße Tierversuche auf den Markt gebracht worden war, wurde die „Notwendigkeit” von Tierversuchen deutlich. Diese Katastrophe, bei der über 100 Menschen starben, weil sie ein Sulfanilamidpräparat einnahmen, das mit einem giftigen Lösungsmittel hergestellt worden war, führte 1938 zur Verabschiedung des Federal Food, Drug, and Cosmetic Act, der vorschreibt, dass Arzneimittel vor ihrer Markteinführung an Tieren auf ihre Sicherheit getestet werden müssen.
84 Jahre später haben sich die FDA-Gesetze zu Tierversuchen mit der Einführung des FDA Modernization Act 2.0 erheblich verändert. Die Senatoren Rand Paul und Cory Brooker sowie der Abgeordnete Vern Buchanan haben den Gesetzentwurf Anfang 2022 eingebracht, und er wurde im September einstimmig verabschiedet. Das Gesetz zielt darauf ab, Innovationen zu beschleunigen und sicherere, wirksamere Medikamente schneller auf den Markt zu bringen, indem bürokratische Hürden abgebaut werden, die durch die aktuelle Wissenschaft nicht gestützt werden. Es handelt sich nicht um ein Verbot von Tierversuchen, sondern es ermöglicht Unternehmen, andere Testmethoden zu verwenden, um Medikamente ohne den Einsatz von Tieren zuzulassen.
Alternativen zu Tierversuchen
In den letzten zehn Jahren haben Wissenschaftler unermüdlich daran gearbeitet, alternative Testmethoden zu entwickeln, die nicht nur humaner sind, sondern auch genauere Ergebnisse liefern, die auf den Menschen übertragen werden können. Von der Verwendung menschlicher Zellen und Gewebe in vitro über fortschrittliche Computermodellierungstechniken bis hin zum Einsatz freiwilliger Probanden revolutionieren diese Alternativen die Art und Weise, wie Medikamente entwickelt und getestet werden.
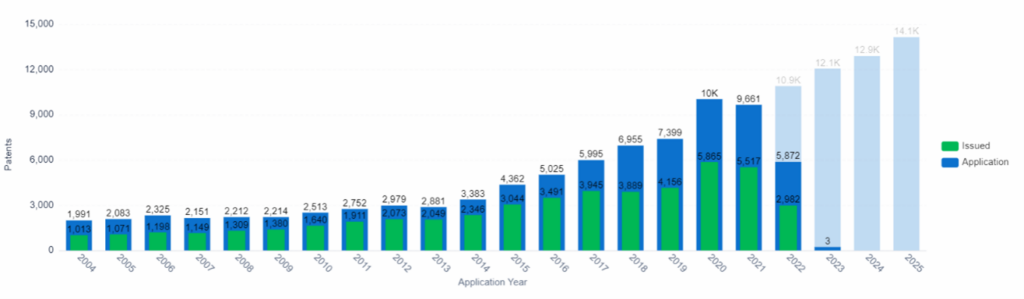
Trend bei Patentanmeldungen und -erteilungen, Organ-on-Chip, PatSnap Insights (Hinweis: Die Daten ab 2022 sind aufgrund der 18-monatigen Verzögerung bei der Einreichung unvollständig).
In diesem Abschnitt tauchen wir ein in die spannende Welt alternativer Testmethoden und stellen die modernsten Techniken vor, die von führenden Pharmaunternehmen eingesetzt werden, um ihre Abhängigkeit von Tierversuchen zu verringern.
Dieser Artikel wurde mithilfe unseres KI-gestützten Discovery-Produkts zusammengestellt, das Milliarden von Patent- und Nicht-Patent-Datenpunkten miteinander verknüpft. Erhalten Sie die technologischen Einblicke und Wettbewerbsinformationen, die Sie benötigen.
Probieren Sie Discovery kostenlos aus
FDA-Alternative zu Tierversuchen Nr. 1: In-vitro-Tests
In-vitro-Pharmakologie ist der Prozess der Durchführung von Arzneimittelversuchen an Mikroorganismen und Zellen außerhalb ihrer normalen biologischen Umgebung (z. B. Tumorzellen in einer Petrischale). Dies ist eine der wichtigsten Methoden, mit denen Forscher Daten zur Wirksamkeit und Sicherheit von Arzneimittelkandidaten gewinnen. In der Phase der Leitstrukturoptimierung bei der Arzneimittelentwicklung kann die In-vitro-Pharmakologie zeitnah hochpräzise Daten liefern, anhand derer die für die jeweilige Erkrankung am besten geeignete Verbindung identifiziert werden kann. Nur die Wirkstoffe, die diese Phase bestehen, gelangen in die präklinische Testphase.
Weitere Beispiele für den Einsatz der In-vitro -Pharmakologie sind:
- Daten zur Sicherheit und Toxizität einer Verbindung sammeln
- Um mögliche nachteilige Auswirkungen frühzeitig im Prozess zu erkennen
- Leitfaden für präklinische In-vivo -Toxizitäts- und Sicherheitsstudien auf der Grundlage von Profilverbindungen.
- Vorhersage der Wirksamkeit und Effizienz des Wirkstoffs gegen die ausgewählte Krankheit.
- Verstehen Sie die Pharmakokinetik und Pharmakodynamik des Wirkstoffs.
- Untersuchen Sie den Wirkmechanismus des Wirkstoffs genauer.
- Biosimilar-Aktivität bewerten.
Der Markt für In-vitro-Toxikologietests wird in den nächsten Jahren voraussichtlich explosionsartig wachsen und bis 2028 einen Wert von unglaublichen 16,5 Millionen US-Dollar erreichen, mit einer durchschnittlichen jährlichen Wachstumsrate (CAGR) von 6,5 % zwischen 2022 und 2028. Aber was treibt dieses Wachstum an?
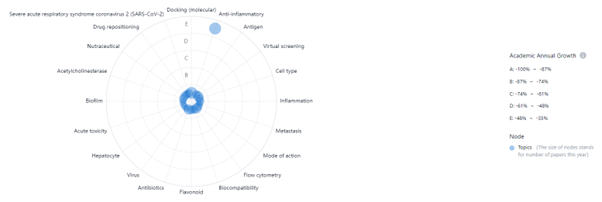
Neue Technologien, In-vitro-Toxikologie, PatSnap Discovery
Es ist eine Kombination verschiedener Faktoren, von den neuesten technologischen Fortschritten bis hin zu den zunehmenden ethischen Bedenken hinsichtlich Tierversuchen. Hinzu kommen die hohen Kosten traditioneller Tierversuche und die steigenden Forschungs- und Entwicklungsausgaben, um Toxizität frühzeitig im Arzneimittelentwicklungsprozess zu erkennen. Damit wird deutlich, dass In-vitro-Toxikologietests eine praktikable Alternative darstellen.
FDA-Alternative zu Tierversuchen Nr. 2: Miniaturorgane:
Organs-on-a-Chip, die durch das Züchten menschlicher Zellen auf Kunststoffgerüsten hergestellt werden, sind die am häufigsten verwendeten „Miniatur“-Organe. Diese winzigen Strukturen ahmen die Funktionen von Organen wie Herz, Leber, Nieren und Lunge nach. Forscher nutzen diese Strukturen, um zu untersuchen, wie Flüssigkeiten durch die Organe fließen, und simulieren dabei den Blutfluss und die Flüssigkeitsverfolgung durch Gewebe. Da beispielsweise die Leber eine wichtige Rolle im Stoffwechsel spielt, kann eine Miniaturleber verwendet werden, um die Toxizität von Medikamenten zu testen, indem die Schädigung der Zellen im System beobachtet wird.
Donald Ingber, Bioingenieur an der Harvard University, entwickelte die Organchip-Technologie und ging eine Partnerschaft mit Emulate ein. Er veröffentlichte eine Studie über den Erfolg der Chips, in der festgestellt wurde, dass die Leberchips 87 % einer Vielzahl von Medikamenten korrekt identifizierten, die nach Tierversuchen, die aufgrund von Lebertoxizität fehlgeschlagen waren, in die klinische Testphase am Menschen gingen. Die Chips meldeten auch keine nicht toxischen Medikamente fälschlicherweise als toxisch.
Der Markt für Organ-on-Chip-Geräte wird in den kommenden Jahren voraussichtlich ein deutliches Wachstum verzeichnen. Im Jahr 2021 wurde der Markt auf 150,3 Millionen US-Dollar geschätzt und soll bis 2029 einen Wert von 1.427,4 Millionen US-Dollar erreichen, was einer durchschnittlichen jährlichen Wachstumsrate (CAGR) von 28,25 % im Prognosezeitraum entspricht. Dieses Wachstum ist auf Faktoren wie die steigende Nachfrage nach Organ-on-Chip-Geräten in der Gesundheitsbranche und die zunehmende Anzahl klinischer Studien zurückzuführen, in denen diese Geräte zur Untersuchung der Toxizität von Arzneimitteln und Kosmetika sowie zum Vergleich der Ergebnisse zwischen menschlichen und tierischen Probanden eingesetzt werden.
FDA-Alternative zu Tierversuchen Nr. 3: Computermodellierung
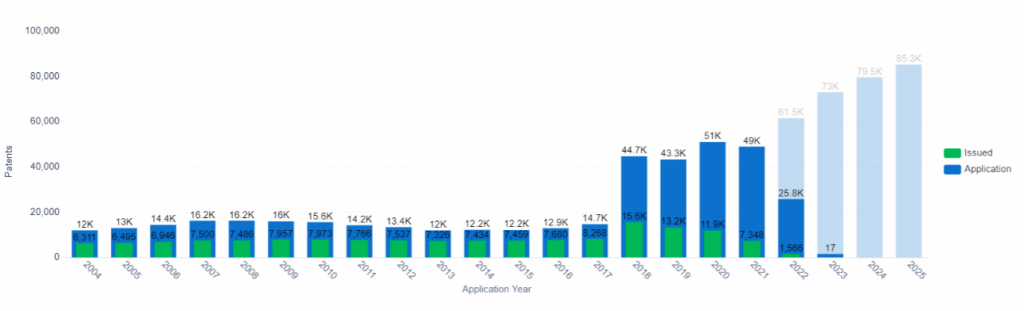
Trends bei Patentanmeldungen und -erteilungen, Computermodellierung, PatSnap Insights (Hinweis: Die Daten ab 2022 sind aufgrund der 18-monatigen Verzögerung bei der Einreichung unvollständig).
Die Verwendung von Daten im Arzneimittelentwicklungsprozess nimmt zu. Forscher nutzen Computermodelle, um große Datenmengen zu analysieren und so die Auswirkungen von Wirkstoffen auf Organismen vorherzusagen.
Ein Team unter der Leitung von Hao Zhu, außerordentlicher Professor für Chemie an der Rutgers University, hat einen Algorithmus entwickelt, der Daten aus chemischen Datenbanken extrahiert und getestete und ungetestete Verbindungen vergleicht, um strukturelle Ähnlichkeiten zu identifizieren und möglicherweise ihren Wirkmechanismus vorherzusagen. Studien, wie beispielsweise eine der John Hopkins University, haben gezeigt, dass die Verwendung von Algorithmen für die Vorhersage der Toxizität vorteilhafter sein kann als Tierversuche. So ergab beispielsweise eine Studie der University of Oxford aus dem Jahr 2018, dass Computersimulationen mit einer Genauigkeit von 89 bis 96 % bei der Vorhersage des klinischen Risikos von arzneimittelinduzierten Arrhythmien besser abschnitten als Tierversuche.
Das Marktwachstum im Bereich der computergestützten Wirkstoffforschung wird zwischen 2022 und 2030 voraussichtlich 7,5 Millionen US-Dollar einbringen, mit einer durchschnittlichen jährlichen Wachstumsrate (CAGR) von 11,48 %. Zu den Faktoren, die dieses Wachstum vorantreiben, gehören chronische, unbekannte und seltene Krankheiten, für die es derzeit keine wirksamen Behandlungsmethoden gibt oder die nur begrenzte Behandlungsmöglichkeiten bieten.
FDA-Alternative zu Tierversuchen Nr. 4: Studien mit freiwilligen Probanden
Ist es wirklich ethisch vertretbar, freiwillige Probanden als Testpersonen für Arzneimittelversuche zu verwenden? Das ist umstritten. Dank technologischer Fortschritte wird dies jedoch immer sicherer. So können beispielsweise hochentwickelte Scanner, wie sie für Gehirnscans verwendet werden, den Verlauf und die Behandlung von Hirnerkrankungen überwachen.
Dadurch können diese Geräte auch Einblicke in die Gehirnfunktion liefern, was besonders bei der Erforschung von Ernährung, Drogenabhängigkeit oder Schmerzempfinden nützlich ist. Nach Abschluss der Untersuchung werden die Ergebnisse mit denen gesunder Probanden verglichen, wodurch ein umfassendes Verständnis darüber gewonnen wird, wie sich Behandlungen auf den menschlichen Körper auswirken.
FDA-Alternative zu Tierversuchen Nr. 5: Mikrodosierung
Ein weiterer Aspekt der „präklinischen Studien am Menschen“ ist die Mikrodosierung. Dabei handelt es sich um sorgfältig kontrollierte Formen von Studien am Menschen, die die Gesundheit der Teilnehmer nicht gefährden. Bei der Mikrodosierung wird menschlichen Freiwilligen ein neues Medikament in sehr geringen Dosen verabreicht, sodass es keine großen physiologischen Auswirkungen hat, aber dennoch genug von der Substanz im Körper vorhanden ist, um die Zellen zu beeinflussen. Diese Art von Tests wird durchgeführt, um nicht wirksame Medikamente in einem frühen Stadium auszusortieren und so Geld für teure Tierversuche mit Wirkstoffen zu sparen, die zum Scheitern verurteilt sind. Dieser Ansatz hat sich als sicher und wirksam erwiesen und wird von vielen Pharmaunternehmen angewendet, um ihren Medikamentenentwicklungsprozess zu optimieren.
Mikrodosierungsstudien bieten mehrere strategische Vorteile, wie z. B. die Beseitigung von Unstimmigkeiten oder Unzulänglichkeiten in präklinischen Daten, die effiziente Überleitung in die Humanprüfung mit begrenzten Ressourcen und die Beschleunigung der Arzneimittelentwicklung für gefährdete Bevölkerungsgruppen. Der Hauptvorteil dieser Phase-0-Studien besteht in den Daten zur Pharmakodynamik (PD) und zum Wirkmechanismus (MOA), die sie liefern und die den Arzneimittelentwicklungsprozess unterstützen.
FDA-Alternative zu Tierversuchen Nr. 6: Menschliche Gewebeproben (Ex Vivo)
Ex vivo bezieht sich auf die Verwendung von ganzen Geweben zur Vorhersage der Wirksamkeit und Sicherheit von Arzneimitteln. Tests an menschlichem Gewebe werden häufig im Arzneimittelentwicklungsprozess eingesetzt, um zu verstehen, wie sich Wirkstoffe auf den Menschen auswirken. Krankheiten wie Diabetes und Krebs können sowohl bei Menschen als auch bei Tieren auftreten, aber es gibt Unterschiede, die zu Diskrepanzen zwischen den Ergebnissen von Tierversuchen und denen von Tests am Menschen führen können.
Menschliche Gewebeproben können stammen aus:
- Chirurgisches Restmaterial: Bei Operationen kann Gewebe zur diagnostischen Untersuchung eingeschickt werden. Wenn Restmaterial übrig bleibt, kann der Pathologe entscheiden, ob es für Forschungszwecke gespendet werden kann.
- Transplantationsgewebe: Wenn es Gründe gibt, warum ein Organ nicht für eine Transplantation verwendet werden kann, kann es für Forschungszwecke verwendet werden.
- Biopsiematerial: Dieses Material wird direkt von Patienten oder Freiwilligen gespendet.
Frische Gewebeproben werden hauptsächlich in späten Phasen der präklinischen Prüfung oder der Leitstrukturoptimierung verwendet, um festzustellen, ob zellbasierte oder tierische Daten auf den Menschen übertragbar sind. Forscher können diese Proben auch verwenden, um zu untersuchen, ob ähnliche Signalwege aktiviert werden und ob bestimmte Biomarker vorhanden sind, die auf eine Wirksamkeit hinweisen. Die Verwendung menschlicher Gewebeproben für Tests in späteren Entwicklungsphasen kann Pharmaunternehmen erhebliche Kosten einsparen, da die Ausfallraten in diesen Phasen hoch sind.
Der weltweite Markt für Gewebediagnostik hatte 2022 einen Wert von 37,8 Milliarden US-Dollar und wird bis 2032 voraussichtlich 122,7 Milliarden US-Dollar erreichen, was einer durchschnittlichen jährlichen Wachstumsrate (CAGR) von 12,5 % entspricht. Der Haupttreiber für dieses Wachstum in den nächsten 10 Jahren ist die zunehmende Alterung der Bevölkerung. Die Studie „World Population Ageing” der Vereinten Nationen prognostiziert, dass die Zahl der Menschen über 65 bis 2050 1,6 Milliarden erreichen wird. Mit der Alterung der Bevölkerung nehmen Krankheiten wie Krebs, Diabetes und Herz-Kreislauf-Erkrankungen zu, was wiederum die Nachfrage nach neuen Gewebediagnostik-Therapien erhöht.
Fazit: Tierversuche könnten aussterben
Mit der Verabschiedung des FDA Modernization Act 2.0 haben Pharmaunternehmen nun die Möglichkeit, Therapeutika ohne den Einsatz von Tieren zu entwickeln. Ein größeres öffentliches Bewusstsein dafür, welche Medikamente an Tieren getestet werden und welche nicht, wird wahrscheinlich zu einer Veränderung des Verbraucherverhaltens führen. Dies bietet eine bedeutende Chance für die weitere Entwicklung und das gestiegene Vertrauen in alternative Testmethoden.
Nutzen Sie die Leistungsfähigkeit KI-gestützter Erkenntnisse, um in Forschung und Entwicklung immer einen Schritt voraus zu sein! Testen Sie unsere innovative Lösung Synapse kostenlos und revolutionieren Sie noch heute die Forschungs- und Entwicklungsarbeit Ihres Life-Science-Unternehmens.



